Die Markteintrittspreise von neuen Arzneimitteln steigen seit Jahren massiv an. Im Jahr 2014 sorgte das Pharmaunternehmen Gilead Sciences mit der Markteinführung des hochwirksamen Hepatitis-C-Medikaments Sovaldi (Sofosbuvir) für Empörung: Eine einzige Tablette Sovaldi kostete bereits 637,70 Euro. Die Jahrestherapiekosten beliefen sich damit auf unglaubliche 85 000 Euro. Gilead Sciences wurde vielerorts scharf kritisiert, ihnen wurde gar Machtmissbrauch vorgeworfen [1]. Der „stern“ analysierte die tatsächlich entstandenen Kosten für das Pharmaunternehmen und errechnete, dass Gilead für sein Medikament von den Krankenkassen das 30-Fache verlangte. Gäbe es ähnliche Aufschläge in anderen Branchen, „würde ein Liter Milch beispielsweise 18 Euro, ein hochwertiges Smartphone 10.000 Euro kosten“ [1].
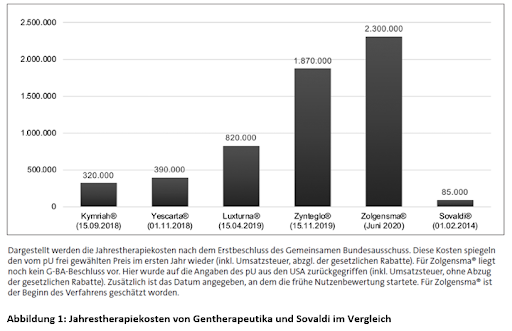
Mittlerweile ist die Aufregung um Sovaldi jedoch Schnee von gestern. Neue Gentherapeutika haben die Messlatte weiter in die Höhe getrieben. Das von Novartis entwickelte Zolgensma schleust über einen Vektorvirus das bei der spinalen Muskelatrophie defekte Gen SMN1 in die Zellen ein. Es soll bereits nach einer einzigen Anwendung zu einer nachhaltigen Verbesserung der motorischen Entwicklung führen. Ohne Behandlung führt die spinale Muskelatrophie in den ersten zwei Lebensjahren zum Tod. Eine Dosis Zolgensma kostet in Deutschland 2,2 Millionen Euro. Es gilt als das teuerste Medikament der Welt [2]. Doch es bleibt fraglich, ob dies lange so bleiben wird: Die Preisentwicklung der letzten Jahre bei neu zugelassenen Medikamenten spricht für sich (siehe Abbildung 1).
Aber wie werden die Preise für neue Medikamente überhaupt festgelegt?
In Deutschland können Anbieter von rezeptfreien Arzneimitteln die Preise frei bestimmen. Für rezeptpflichtige Präparate gilt seit 2011 das AMNOG-Verfahren (Arzneimittelmarktneuordnungsgesetz) [6]. Demnach darf der Hersteller im ersten Zulassungsjahr den Preis eines patentgeschützten Arzneimittels zunächst frei festlegen. In dieser Zeit wird das Medikament vom Gemeinsamen Bundesausschuss (G-BA) hinsichtlich seines Zusatznutzens beurteilt [3]. Hat es keinen Zusatznutzen, muss sich der Hersteller an den Preisen vergleichbarer Präparate orientieren. Kann jedoch ein Mehrwert festgestellt werden, wird über mehrere Monate zwischen Vertretern des Unternehmens und dem GKV-Spitzenverband über den neuen Preis verhandelt [4]. Grundlage für diese Verhandlungen sind die bisher üblichen Therapiekosten, der ermittelte Zusatznutzen (z.B. eine bessere Wirkung oder weniger Nebenwirkungen) der neuen Therapie und die Vergleichspreise in anderen Ländern [4]. Für das rekordteure Gentherapeutikum Zolgensma wird beispielsweise Ende dieses Jahres der Preis neu verhandelt, da das erste Zulassungsjahr vorbei ist.
Dabei bleibt jedoch unklar, wie sehr das AMNOG-Verfahren tatsächlich zu einer Preissenkung beiträgt. Durchschnittlich werden die Preise gegenüber dem Einführungspreis im Rahmen der Verhandlungen um ein Viertel gesenkt. Es ist allerdings nicht unwahrscheinlich, dass Hersteller die Preise deshalb bereits im Vorhinein höher ansetzen [4]. Hinzu kommt, dass die tatsächlichen Preise in anderen Ländern nicht transparent sind. Es ist üblich, dass Hersteller und Krankenkassen spezielle Rabatte aushandeln, die aber streng vertraulich bleiben. Der Listenpreis des Medikaments ändert sich dadurch also nicht [5].
External Price Referencing
Dieser Listenpreis ist jedoch nicht nur für das deutsche AMNOG-Verfahren von großer Bedeutung, sondern auch für die Preisverhandlungen in zahlreichen anderen Ländern (z.B. in allen EU-Mitgliedsstaaten außer Schweden), denn sie nutzen die Marktpreise im Ausland als Basis zur Preisfestlegung im eigenen Land. Diese Praxis nennt sich External Price Referencing (EPR). Da die geheimen Rabatte nicht im Listenpreis berücksichtigt werden, kommt es zu einer verzerrten Abbildung der Verkaufspreise [5]. Die Daten zu den Preisnachlässen sind nicht öffentlich zugänglich [4]. So sind beispielsweise die Vertreter des GKV-Spitzenverbandes bei den Verhandlungen im Rahmen des AMNOG-Verfahrens auf die Richtigkeit der Angaben der Hersteller angewiesen. Letztendlich ist eine unabhängige Prüfung der Einkaufspreise für ein bestimmtes Medikament mit der Intransparenz des heutigen Systems nicht möglich.
Aus der EPR-Strategie resultieren noch weitere Einflüsse auf den europäischen Medikamentenhandel. Um den Referenzpreis ihres neuen Produkts möglichst hochzuhalten, bringen Hersteller ihr Medikament bevorzugt in Ländern mit hohen Preisniveaus auf den Markt. Die Markteinführung in anderen Ländern wird systematisch verzögert oder gar verhindert [5]. In Deutschland erhöht die Möglichkeit der freien Preiswahl der Hersteller im ersten Zulassungsjahr den Referenzpreis. Hierzulande sind Arzneimittel deshalb oft früher verfügbar als in anderen europäischen Ländern.
Andererseits können die vertraulich ausgehandelten Preisnachlässe auch eine Chance für Länder mit geringerem Preisniveau darstellen. Durch hohe Rabatte könnte die Medikamentenversorgung dieser Länder gewährleistet werden, ohne den Listenpreis negativ zu beeinflussen [5].
Das Dilemma
Es liegt also einerseits im wirtschaftlichen Interesse der Länder einen möglichst niedrigen Erstattungsbetrag auszuhandeln. Doch aus preisgünstigen Einkaufspreisen für Medikamente können auch Versorgungsengpässe resultieren. Denn in diesem Falle lohnt es sich für Händler, die Arzneimittel in andere Länder weiterzuverkaufen [7]. Hinzu kommt, dass hohe Erstattungsbeträge einen frühen Zugang zu neuen, womöglich besseren Arzneimitteln sichern können. Dies liegt ebenfalls im Interesse der Bevölkerung. Wir befinden uns also stetig in einem Spannungsfeld zwischen Kostenreduktion und der Gewährleistung einer ausreichenden Patientenversorgung [8].
Lösungsansätze
Wie kann also die Explosion der Medikamentenpreise gebremst und ein gerechter Zugang zu fair bepreisten Arzneimitteln garantiert werden?
Mehr Transparenz
Simulationen zeigen, dass Kosten gespart werden könnten, wenn die tatsächlich gezahlte Beträge und nicht die Listenpreise als Referenz für neue Verhandlungen genutzt werden könnten [8]. Dazu müsste nicht zwingend eine europaweite Preistransparenz bestehen. Schon kleinere Zusammenschlüsse von mehreren Ländern, innerhalb derer Preisnachlässe offen kommuniziert werden, hätten einen positiven Effekt. Heute sind wir noch weit davon entfernt: nur Österreich veröffentlicht derzeit für welche Medikamente Rabatte gewährt wurden, nicht aber über welche Höhe [5].
Obergrenze für Jahrestherapiekosten
Ebenfalls könnte eine Deckelung des Erstattungsbetrages durch eine festgelegte Obergrenze abhängig von Patientengruppe und Behandlungssituation, zu einer Kostensenkung führen [9]. Dies wirft jedoch eine wichtige Frage auf: Wieviel ist die Gesellschaft bereit zu zahlen? Sind 2,2 Millionen Euro für das Leben eines Kindes zu viel? Diese Fragen sind nicht rein wirtschaftlich zu betrachten und müssen unter anderem auch von Medizinethikern beantwortet werden. Wichtig ist es auch zu bedenken, dass nicht die sündhaft teuren, aber selten verschriebenen Gentherapeutika die Ausgaben der Krankenkassen in die Höhe treiben, sondern viel eher die modernen Krebstherapien, die viel mehr Patienten benötigen [4].
Fest steht: Langfristig muss sich etwas ändern! Dabei gibt es jedoch kein „one size fits all“ Modell [10]. Stattdessen sollten verschiedene Methoden kombiniert werden. Nur mit mehr Transparenz und einer verstärkten Zusammenarbeit der EU-Staaten kann eine faire Versorgung aller Bürger gewährleistet werden.
Weiterlesen:
Spiegel Bericht zur einheitlichen Pharma Strategie
Stern Bericht: Deutschland zweitteuerstes Land bei Arzneimitteln
Stern Bericht: Wie Pharmaindustrie ihre Marktmacht missbraucht
Zeit Artikel: Medikamenten Preisbildung und Entwicklung der Kosten
QUELLEN
[1] https://www.stern.de/gesundheit/wie-die-pharmaindustrie-ihre-marktmacht-missbraucht-6510110.html
[2] https://www.wissensschau.de/genom/gentherapie_zolgensma_spinale_muskelatrophie.php
[3] https://www.vfa.de/de/wirtschaft-politik/abcgesundheitspolitik/amnog-schnell-erklaert.html
[5] Vogler, S., Paris, V., Ferrario, A., Wirtz, V. J., de Joncheere, K., Schneider, P., Pedersen, H. B., Dedet, G., & Babar, Z.-U.-D. (2017). How can pricing and reimbursement policies improve affordable access to medicines? lessons learned from European countries. Applied Health Economics and Health Policy, 15(3), 307–321. https://doi.org/10.1007/s40258-016-0300-z
[6] https://www.test.de/medikamente/Medikamente-im-Test-5418254-5418291/
[7] https://www.pharma-fakten.de/news/details/690-arzneimittelpreise-im-europaeischen-vergleich/
[8] Vogler, S., Lepuschütz, L., Schneider, P., & Stühlinger, V. (2015). (rep.). Study on enhanced cross-country coordination in the area of pharmaceutical product pricing. European Commission.
[9] Natalie, K. (2020). Denksport – Preise für neue Arzneimittel in Schach halten. Gesundheits- Und Sozialpolitik, 74(3), 49–53. https://doi.org/10.5771/1611-5821-2020-3-4
[10] World Health Organization. Regional Office for Europe. (2018). Medicines reimbursement policies in Europe. World Health Organization. Regional Office for Europe. https://apps.who.int/iris/handle/10665/342220
Abbildung 1:
Natalie, K. (2020). Denksport – Preise für neue Arzneimittel in Schach halten. Gesundheits- Und Sozialpolitik, 74(3), 49–53. https://doi.org/10.5771/1611-5821-2020-3-4
